Rumus Empiris dan Rumus Molekul – Pengantar
Setiap senyawa kimia dapat dinyatakan dengan rumus kimia yang menunjukkan jumlah relatif atom-atom unsur dalam senyawa tersebut. Rumus kimia dibedakan menjadi dua jenis, yaitu rumus molekul dan rumus empiris. Rumus molekul dari suatu senyawa menunjukkan jumlah atom sebenarnya dari masing-masing unsur dalam satu molekul senyawa tersebut. Jadi, rumus molekul dari karbon dioksida adalah CO2; setiap molekul karbon dioksida terdiri dari 1 atom karbon dan 2 atom oksigen. Rumus molekul dari asam askorbat (vitamin C) adalah C6H8O6; setiap molekul asam askorbat terdiri dari 6 atom karbon, 8 atom hidrogen, dan 6 atom oksigen.
Rumus empiris dari suatu senyawa menunjukkan jumlah atom relatif dari masing-masing unsur dalam molekul senyawa tersebut dengan rasio (perbandingan) bilangan bulat paling sederhana. Sebagai contoh, rumus empiris dari asam askorbat adalah C3H4O3, di mana perbandingan jumlah atom karbon, hidrogen, dan oksigen adalah 3 : 4 : 3. Rumus empiris dari karbon dioksida sama dengan rumus molekulnya, yaitu CO2, sebagaimana perbandingan jumlah atom karbon dan oksigen yang paling sederhana adalah 1 : 2. Secara umum, rumus molekul akan lebih penting dan dipilih dibanding rumus empiris, sebab informasi dari rumus molekul lebih mendetail.
Namun, dalam beberapa padatan dan cairan, tidak dijumpai adanya molekul kecil yang dapat dipisahkan satu sama lain, sehingga rumus kimia yang memiliki makna penting hanyalah rumus empirisnya. Sebagai contoh, padatan garam natrium klorida yang memiliki rumus empiris NaCl. Dalam padatan NaCl, terdapat gaya tarik-menarik yang sangat kuat antar atom Na dan atom Cl, namun mustahil untuk membedakan gaya-gaya yang bekerja antar “molekul” NaCl sebab semua gaya tarik yang bekerja pada atom Na dan atom Cl dalam “satu molekul” NaCl dengan atom-atom Na dan Cl tetangga sama besar. Oleh karena itu, natrium klorida dinyatakan dengan rumus empiris yang disebut juga sebagai unit rumus (formula unit) NaCl, bukan “sebuah molekul NaCl”. Ada banyak padatan lainnya yang juga hanya dapat dirumuskan dalam bentuk unit rumus, seperti silikon dioksida (SiO2), kalsium fluorida (CaF2), dan zink sulfida (ZnS).
Rumus Empiris dan Kadar Unsur dalam Senyawa
Kadar unsur dalam senyawa umumnya dinyatakan dalam persen massa unsur tersebut terhadap massa senyawa. Kadar unsur juga dapat dinyatakan sebagai massa unsur dalam 1 mol senyawa dibagi dengan massa molar senyawa tersebut lalu dikali dengan 100 persen. Massa unsur dalam 1 mol senyawa sama dengan jumlah mol unsur (n) dalam 1 mol senyawa dikalikan dengan massa molar unsur.
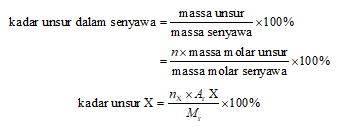
Contoh Soal Kadar Unsur dalam Senyawa dan Pembahasan
Tentukan kadar masing-masing unsur dalam senyawa aspirin (C9H8O4).
Jawab:
Dalam senyawa C9H8O4 terdapat tiga unsur, yaitu C, H, dan O.
kadar unsur C =
kadar unsur H =
kadar unsur O =
Rumus empiris senyawa dapat diketahui dari kadar unsur-unsur penyusun senyawa dengan mengkonversi kadar unsur menjadi rasio mol unsur. Hal ini dapat dilakukan dengan mengasumsikan terdapat 100 gram sampel senyawa sehingga massa masing-masing unsur dapat ditentukan dari kadar unsur, lalu massa unsur dibagi dengan massa molar unsur hingga diperoleh jumlah mol masing-masing unsur. Selanjutnya, jumlah mol masing-masing unsur dibandingkan hingga diperoleh rasio dalam bilangan bulat yang paling sederhana. Rasio mol unsur-unsur yang menunjukkan jumlah relatif atom unsur dalam senyawa inilah yang merupakan rumus empiris.
Contoh Soal Rumus Empiris dan Pembahasan
Dari hasil analisis unsur pada senyawa pirimidin, diperoleh kadar unsur karbon 60%, hidrogen 5%, dan sisanya nitrogen. Tentukanlah rumus empiris senyawa primidin.
Pembahasan:
Dalam senyawa pirimidin terdapat tiga unsur, yaitu C (60%), H (5%), dan N (35% = 100% – 60% – 5%).
Mula-mula, kadar unsur dikonversi menjadi jumlah mol dengan mengasumsikan bahwa terdapat 100 g senyawa:
jumlah mol C =
jumlah mol H =
jumlah mol N =
Rasio mol unsur C : H : N yaitu (kedua ruas dibagi 2,5)
Jadi, rumus empiris senyawa pirimidin yaitu C2H2N.
Rumus Molekul dan Rumus Empiris
Rumus molekul yang menunjukkan jumlah atom sebenarnya dari suatu molekul senyawa dapat sama dengan rumus empiris ataupun kelipatan bilangan bulat darinya. Namun, untuk mengetahui rumus molekul dari rumus empiris, perlu diketahui massa molar senyawa tersebut terlebih dahulu.
rumus molekul = (rumus empiris)x
massa molar rumus molekul = x . massa molar rumus empiris
Mr rumus molekul = x . Mr rumus empiris
di mana x adalah bilangan bulat positif (1, 2, 3, …)
Contoh Soal Rumus Empiris dan Rumus Molekul dan Pembahasan
Kafein (Mr = 194) adalah zat stimulan yang banyak ditemukan dalam kopi, teh, dan minuman ringan. Analisis unsur dari senyawa kafein menunjukkan terdapat 49,47% karbon, 5,19% hidrogen, 28,86% nitrogen, dan 16,48% oksigen. Tentukanlah rumus molekul senyawa kafein.
Jawab:
Dalam senyawa pirimidin terdapat empat unsur, yaitu C (49,47%), H (5,19%), N (28,86%), dan O (16,48%).
Mula-mula, kadar unsur dikonversi menjadi jumlah mol dengan mengasumsikan bahwa terdapat 100 g senyawa:
jumlah mol C = nC =
jumlah mol H = nH =
jumlah mol N = nN =
jumlah mol O = nO =
Rasio mol unsur C : H : N : O yaitu (kedua ruas dibagi 1,03_
Jadi, rumus empiris senyawa kafein yaitu C4H5N2O.
Mr (C4H5N2O) = (4 x Ar C) + (5 x Ar H) + (2 x Ar N) + (1 x Ar O)
= (4 x 12) + (5 x 1) + (2 x 14) + (1 x 16) = 97
Mr rumus molekul = x . Mr rumus empiris
194 = x . 97
x = 2
Oleh karena rumus molekul = (rumus empiris)x, maka rumus molekul = (C4H5N2O)2 = C8H10N4O2.
Jadi, rumus molekul senyawa kafein adalah C8H10N4O2.
Referensi
Atkins, Peter & Jones, Loretta. 2010. Chemical Principles: The Quest for Insight (5th edition). New York: W.H. Freeman & Company
Brown, Theodore L. et al. 2015. Chemistry: The Central Science (13th edition). New Jersey: Pearson Education, Inc.
Chang, Raymond & Goldsby, Kenneth A. 2016. Chemistry (12th edition). New York: McGraw-Hill Education
Johari, J.M.C. & Rachmawati, M. 2009. Kimia SMA dan MA untuk Kelas X Jilid 1. Jakarta: Esis
McMurry, John E., Fay, Robert C., & Robinson, Jill K. 2016. Chemistry (7th edition). New Jersey: Pearson Education, Inc.
Oxtoby, David W., Gillis, H.P., & Campion, Alan. 2012. Principles of Modern Chemistry (7th edition). California: Brooks/Cole, Cengage Learning
Petrucci, Ralph H. et al. 2017. General Chemistry: Principles and Modern Applications (11th edition). Toronto: Pearson Canada Inc.
Purba, Michael. 2006. Kimia 1A untuk SMA Kelas X. Jakarta: Erlangga
Retnowati, Priscilla. 2004. SeribuPena Kimia SMA Kelas X Jilid 1. Jakarta: Erlangga
Silberberg, Martin S. & Amateis, Patricia. 2015. Chemistry: The Molecular Nature of Matter and Change (7th edition). New York: McGraw-Hill Education
Kontributor: Nirwan Susianto, S.Si.
Alumni Kimia FMIPA UI
Materi StudioBelajar.com lainnya:

Leave a Comment